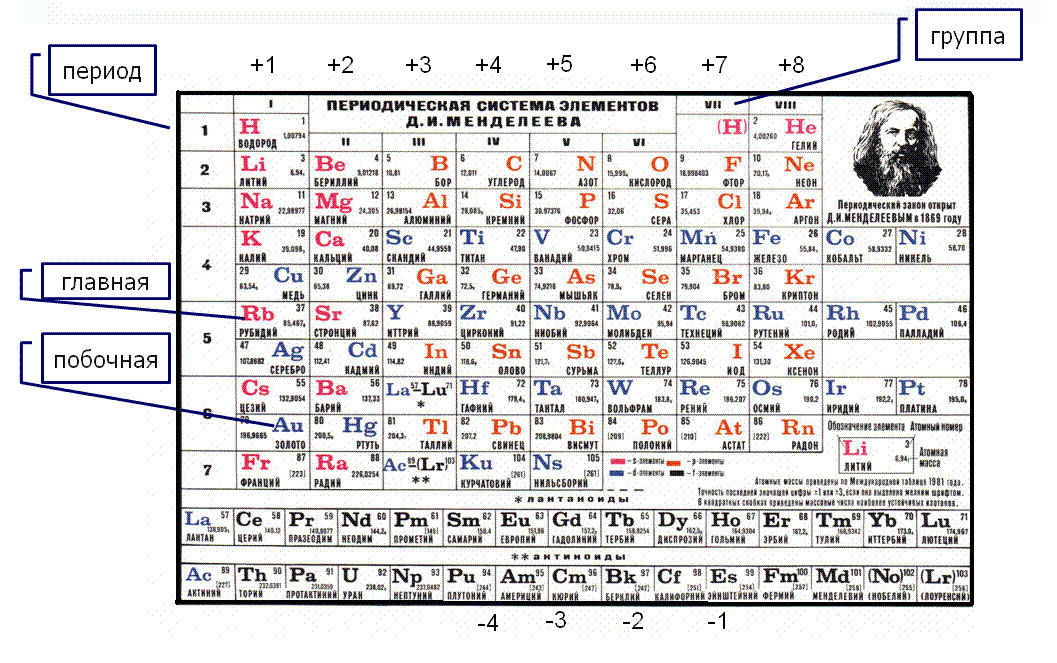
В период попадают элементы с одинаковым числом электронных слоев. Всего 7 периодов. Число элементов в периоде определяется электронным строением квантовых уровней.
1-3 –малые, а остальные большие. В малых периодах находятся s-и р- элементы, а в больших- d-f-элементы.
Группу образуют элементы с одинаковым числом валентных электронов. Она делится на главную (А) и побочную(В).
В главную входят элементы у которых валентные электроны располагаются на внешнем слое (s-, p-).
Металлы могут проявлять положительные (+) степени окисления, а неметаллы могут и отрицательную (-) с.о.
- Высшая положительная степень окисления равна номеру группы.
- Промежуточные степени окисления определяются: № (группы)-2.
- Отрицательная степень окисления определяется №(группы)-8.
В побочную входят элементы, у которых заполняется предвнешний слой (d) или внутренний слой(f). Все d,f- элементы металлы.
f-элементы находятся в 3В подгруппе и занимают 1 клетку либо La (лантаноиды),Ас (актиноиды). Основная их с.о.+3, но может быть и больше.